(1)硅(IV)酞菁二(三己基甲硅烷基氧化物)结构如图所示,基态N原子的空间运动状况有
(3)某种灰硒的晶体为六方晶胞结构,原子排列为无限螺旋链,同一条链内原子效果很强,相邻链之间原子效果较弱,其螺旋链状图、晶胞结构图和晶胞俯视图如下图所示,则相邻链之间的效果力为___________。
-钾和碘的相关化合物在化工、医药、资料等范畴存在广泛的使用,由相应的剖析方法能够得到这些物质的各类数据,答复下列问题。
(3)某晶体具有十分杰出的光学性质,其晶胞结构如如图所示,该立方体晶胞的边长均为0.446nm。
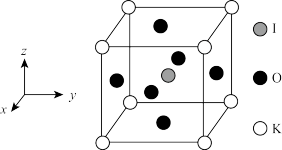
②该晶体中与I原子紧邻的O原子个数为_______,I的原子坐标为_______。

-
(1)Bi与P坐落同主族,基态P原子的价层电子排布式为____。基态Se原子核外电子云概括图呈哑铃形的能级上共有___个电子。
表明,其间m代表参加构成大π键的原子数,n代表参加构成大π键的电子数,则


(5)硒化锌的晶胞如图所示,a点锌原子坐标为(0,0,0),b点锌原子坐标为(0,
-已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数ABCDE。其间A、B、C是同一周期的非金属元素。AC对错极性分子。B、C的氢化物的沸点比它们本家相邻周期元素氢化物的沸点高。E的原子序数为24,ECl能与B、C的氢化物构成六配位的合作物,且两种配体的物质的量之比为2:1,三个氯离子在外界。根据以上情况,答复下列问题:(答题时,A、B、C、D、E用所对应的元素符号表明)
(2)B的氢化物的分子立体构型是_____;其间心原子采纳_______杂化。
(3)写出化合物AC2的电子式为_______;一种由B、C组成的化合物与AC2互为等电子体,其化学式为______。
(2)BeCl2是共价分子,能够以单体、二聚体和多聚体方式存在。它们的结构简式如下,请写出Be的杂化轨迹类型:
-I. 近来,济南大学原长洲教授制备了一种高性能的钾离子电池负极资料(Bi-MOF),反响可简略表明为Bi(NO
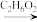
(1)Bi(NO3)3中阴离子的立体构型为_______。基态O原子核外成对电子数与未成对电子数之比为_______。
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为_______。
(3)冠醚是皇冠状的分子,可用不同巨细的空穴适配不同巨细的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子构成的超分子结构如图所示。

(4)铝离子电池的其间一种正极资料为AlMn2O4,其晶胞中铝原子的骨架如图所示。

②以晶胞参数为单位长度树立的坐标系能够表明晶胞中各原子的方位,称作原子分数坐标,如图中原子1的坐标为(
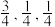
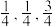
N)是含有一个氮杂原子的六元杂环化合物。能够看作是苯分子中的一个(CH)被N替代的化合物,故又称氮苯,结构如图
(3)一种由Cu、In,Te组成的晶体属四方晶系,晶胞参数和晶胞中各原子的投影方位如图所示,晶胞棱边夹角均为90°。
-已知A、B、C、D、E、F、G七种元素的原子序数顺次递加,前四种元素为短周期元素

坐落元素周期表s区,电子层数与未成对电子数持平;B基态原子中电子占有三种能量不同的原子轨迹,且每轨迹中的电子总数相同;D原子核外成对电子数为未成对电子数的3倍;F坐落第四周期d区,最高能级的原子轨迹内只要2个未成对电子;E的一种氧化物具有磁性;C与G同主族。

的中心原子价电子数与配体供给电子总数之和为18(1个BD分子可供给的电子数为2),则
-
a.快速降温冷却结晶b.常温缓慢冷却结晶c.避光结晶d.拌和e.玻璃棒恰当刮擦试管内壁供给晶核
(4)显色剂显色时会生成一种蓝色沉积,该蓝色沉积的化学名称为:_____,该蓝色沉积中存在的效果力类型有_____。
-江西矿藏资源丰富,其间铁、锰、钛、钒、铜、锌、金、银等储量居全国前3位,有亚洲最大的铜矿和我国最大的铜锻炼基地。请按要求答复下列问题:
(2)向盛装有硫酸铜水溶液的试管里参加氨水,首要生成蓝色沉积,持续滴加氨水,得到深蓝色的通明溶液,向溶液中参加95%的乙醇并用玻璃棒冲突试管壁,分出深蓝色晶体。
②深蓝色晶体中阴离子的空间结构名称是___________,深蓝色都是因为存在___________(配离子化学式),配离子中H-N-H键角___________(填“大于”、“小于”或“等于”)氨气中H-N-H键角。
(4)GaAs是一种重要的半导体资料,晶胞如图1;将Mn掺杂到GaAs的晶体中得到稀磁性半导体资料,晶体结构如图2。已知GaAs晶胞沿
-Pt-硼酸钴是一种高效催化剂,能够在必定程度上完结硝基化合物和醛类化合物进一步组成亚胺。请按要求答复下列问题:
(1)基态Co原子的价电子轨迹表明式是___________,B原子的最低能级原子轨迹电子云形状是___________。

(3)B2O3是硼酸的酸酐,其气态分子结构如图1所示。B2O3遇到热的水蒸气时,反响生成偏硼酸[B3O3(OH)3],其结构如图2所示,该反响中B原子杂化轨迹类型由___________变为___________,偏硼酸分子中各元素电负性由大到小的次序是___________。

(4)常温常压下,硼酸(H3BO3)晶体结构为层状,其二维平面结构如下图所示,1molH3BO3晶体中含有___________mol氢键;请从氢键的视点解说硼酸在冷水中的溶解度小而加热时溶解度增大的原因___________。

-合作物在许多顶级范畴如激光资料、超导资料、抗癌药物的研讨、催化剂的研发、自拼装超分子等方面有广泛的使用。答复下列问题:
经过配位键构成了晶体的骨架。其部分结构如图1,记为I型立方结构。将I型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,基层左后的小立方体g未标出)。
-Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极资料研讨方面的卓越贡献而取得2019年诺贝尔化学奖。答复下列问题:
(1)写出基态Р原子的电子排布式___________,有___________种空间运动状况,占有最高能级的电子云概括图为___________形。
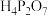

的晶胞结构示意图如(a)所示。其间О环绕Fe和Р别离构成正八面体和正四面体,它们经过共极点、共棱构成空间链结构。每个晶胞中含有