由结构简式可知有机物含有羟基、羧基,可发生替代、氧化、消去、酯化反响,具有酸性,可发生中和反响,以此回答该题.
回答解:(1)由结构简式可知有机物分子式为C4H6O5,故答案为:C4H6O5;
(3)苹果酸中含有羧基、醇羟基,含有羧基,能和Na、NaOH、碳酸氢钠反响,能和醇发生酯化反响,具有醇羟基,能发生酯化反响、氧化反响、消去反响、替代反响,能焚烧,不含不饱和键,所以不能发生水解反响、加聚反响,故答案为:②③;
(4)有机物含有2个羧基、1个羟基,则1mol苹果酸与足量的钠反响最多发生1.5mol氢气,故答案为:1.5mol;
点评本题考察有机物的结构和性质,清晰有机物中官能团及其性质联系是解本题要害,熟练掌握常见有机物的官能团,物质反响条件,条件不同产品不同,标题难度不大.
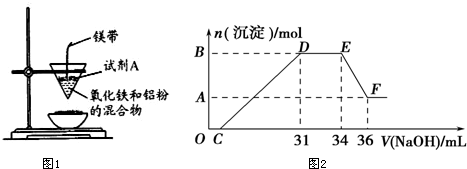
将反响后容器中的剩余固体置于烧杯中,参加100mL稀硝酸,固体彻底溶解,(假定固体悉数溶解后溶液体积不变),反响过程中无气体放出(生动金属可把稀HNO3还原为NH4NO3).向反响后的溶液中缓慢滴加4molL-1的NaOH溶液,发生沉积的物质的量与参加NaOH溶液的体积的联系如图2所示:
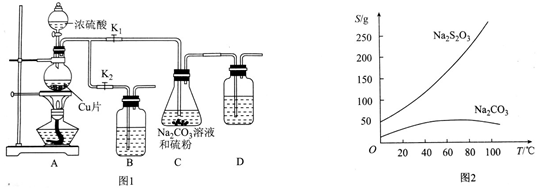
(1)查看设备气密性,按图1所示参加试剂,其间设备B和D中加的是NaOH溶液,设备C中的硫粉应事前研细并用乙醇潮湿,否则会影响下降反响速率.
(2)翻开K1、封闭K2,向圆底烧瓶中参加足量浓硫酸并加热.C中混合液被气流搅动,反响一段时间后,硫粉的量逐步削减.
(3)当C中溶液的pH挨近7时,翻开K2、封闭K1并中止加热.采纳该办法的理由是避免SO2过量,溶液呈现酸性,导致生成的Na2S2O3分化.
(4)将C中的混合液过滤,将滤液通过一系列操作,可得粗产品Na2S2O35H2O.
(5)粗产品中或许含有Na2SO3、Na2SO4等杂质,使用所给试剂规划试验,查验测验产品中是不是真的存在Na2SO4,扼要阐明试验操作,现象和定论:取少数产品溶于足量稀盐酸,静置,取上层清液(或过滤,取滤液),滴加BaCl2溶液,若呈现沉积则阐明含有Na2SO4杂质.
含氯消毒剂给自来水消毒后余氯含量的计划如下:在250ml碘量瓶(或具塞锥形瓶)中放置0.5gKI,加10ml稀硫酸,精确量取活动水样100ml(翻开自来水龙头,待水流数十秒后再取水样)置于碘量瓶,敏捷塞上塞摇摆,见水样呈淡黄色,加1ml淀粉溶液变蓝,则阐明水样中有余氯.再以Cmol/L规范Na2S2O3溶液滴定,至溶液蓝色消失呈无色通明溶液,记下硫代硫酸钠溶液的体积.
(6)若该自来水是以漂白粉消毒,能阐明水样中有余氯的反响离子方程式为ClO-+2I-+2H+=Cl-+I2+H2O.
(7)上述试验,消耗规范Na2S2O3溶液VmL,则自来水样品中余氯量(以游离Cl2核算)为355VCmgL-1.试验中,若“塞上塞摇摆”动作缓慢,则测得成果偏高(填“偏高”“偏低”或“不变”).