(3)⑤处气体混合物主要是氮气和三氧化硫.此时气体经过⑥后不立即进入⑦是因为:
(4)20%的发烟硫酸(SO3的质量分数为20%)1吨需加水吨(保留2位有效数字)才能配制成98%的成品硫酸.
(5)在②处发生1500℃的“不完全燃烧”,即先混入少量干燥空气,然后在③处于700℃下再继续燃烧.试简述这种燃烧方式对环境保护是有利的原因.


(2)该反应为可逆反应,二次催化使尚未反应的SO2尽量催化氧化成SO3,能够更好的降低成本提高原料利用率和保护环境(2分。其中“提高原料利用率”1分,“保护环境” 1分)
(3)通过吸收塔⑥后,混合气体中SO3含量较多,不利于SO2的催化氧化反应进行。(2分。“SO3含量较多”1分,“不利于SO2的催化氧化”1分)
(5)在高温下,空气的氮气和氧气反应生成氮氧化物,有污染。低温下,氮氧化物被还原,生成N2,对环境保护有利。(2分,“生成氮氧化物”1分,“氮氧化物被还原”1分)

;该反应是放热的可逆反应,温度过高平衡逆向移动,不利于 SO3 的生成,且影响催化剂的活性,所以采用等温过程。
(2)通过一次催化炉④不可能将二氧化硫完全氧化成三氧化硫。为充分利用原料,所以设置二次催化炉⑦,使尚未反应的二氧化硫尽量催化氧化成三氧化硫,这对于减少相关成本和环境保护都是必要的。
(3)⑤处的混合气体主要是三氧化硫和氮气及少量的二氧化硫,通过吸收塔⑥后,只能吸收一部分三氧化硫。若将这种含三氧化硫多、二氧化硫少的混合气体直接通入第二个催化炉⑦,这时带入催化剂表面上的三氯化硫的分压比较高,二氧化硫的分压很低,不利于反应进行。
(5)1500℃时,空气中的氮 气和氧气反应生成有毒的氮化物,有污染,若温度较低,如 700℃下,氮氧化物被还原为N2,所以这种燃烧方法对环境保护有利。
考点:本题考查化学流程图的分析、化学方程式的书写、工业操作原因的分析、反应物的计算。
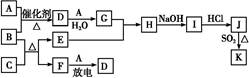
已知:A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出)。请回答下列问题:
(5)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式。
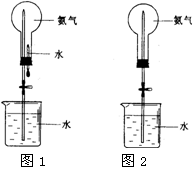
喷泉是一种常见的自然现象,其产生的原因是存在压强差。制取氨气并完成喷泉实验(图中夹持装置均已略去)。
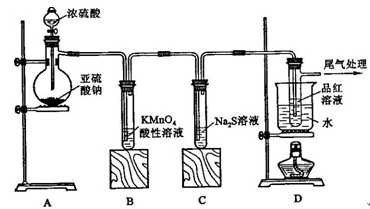
(2)实验过程中,装置B、C中发生的现象分别是、,这些现象分别说明SO2具有的性质是和;装置B中发生反应的离子方程式为;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象;
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
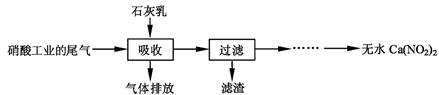

(2)上述工艺中采用气液逆流接触吸收(尾气从吸收塔底部进入,石灰乳从吸收塔顶部喷淋),其目的是;滤渣可循环利用,滤渣的主要成分是(填化学式)。
(3)该工艺需控制NO和NO2物质的量之比接近1︰1。若n(NO):n(NO2)>1︰1,则会导致;若n(NO):n(NO2)<1︰1,则会导致。
(4)生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式。

①若制取11.2 L Cl2(标准状况),则最少应加入MnO2的质量为______g。
②用平衡移动原理解释可用排饱和食盐水法收集氯气的原因。(结合必要的化学用语及文字回答)
③制备氯气时,可用NaOH溶液吸收尾气,下列试剂也可用于吸收氯气的是____(填字母)。
④也可用浓氨水吸收氯气,同时生成一种无污染的气体,反应的化学方程式是_______。
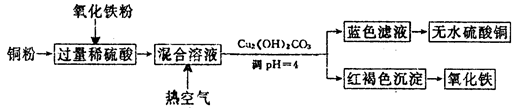
(2)方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:
清洗和制绒是硅晶片制作的重要步骤之一,硅片化学洗涤的最大的目的是除去硅片表面杂质(如某些有机物,无机盐,金属、Si、SiO2粉尘等)。常用的化学清洗剂有高纯水、有机溶剂、双氧水、浓酸、强碱等。其中去除硅的氧化物,通常用一定浓度的HF溶液,室温条件下将硅片浸泡1至数分钟。制绒是在硅片表明产生金字塔形的绒面,增加硅对太阳光的吸收。单晶制绒通常用NaOH,Na2SiO3等混合溶液在75~90℃反应25~35 min,效果良好。
(2)写出晶片制绒反应的离子方程式,对单晶制绒1990年化学家Seidel提出了一种的电化学模型,他指出Si与NaOH溶液的反应,首先是Si与OH一反应,生成SiO44一,然后SiO44一迅速水解生成H4SiO4。基于此原理分析反应中氧化剂为。
(3)本校化学兴趣小组同学,为验证Seidel的理论是不是正确,完成以下实验:
普通玻璃器皿中的水仅因含有从玻璃中溶出的微量的碱便可使粉末状硅在其中缓慢溶解。
在野外环境里,用较高百分比的硅铁粉与干燥的Ca(OH)2和NaOH,点着后焖烧,可剧烈放出H2。
结论:从实验上说明碱性水溶液条件下,H2O可作剂;NaOH作剂,降低反应。高温无水环境下,NaOH作剂。
(4)在太阳能电池表面沉积深蓝色减反膜——氮化硅晶膜。常用硅烷(SiH4)与氨气(NH3)在等离子体中反应。硅烷是一种无色、有毒气体,常温下与空气和水剧烈反应。下列关于硅烷、氮化硅的叙述不正确的是。
A.在使用硅烷时要注意隔离空气和水,SiH4能与水发生氧化还原反应生成H2;
B.硅烷与氨气反应的化学方程式为:3SiH4+4NH3=Si3N4+12H2↑,反应中NH3作氧化剂;
C.它们具有卓越的抗氧化、绝缘性能和隔绝性能,化学稳定性很好,不与任何酸、碱反应;
某金属M的氢氧化物的水合晶体[M(OH)2?xH2O]与Na2CO3混合物共36.800g,加入足量的水后,生成MCO3的白色沉淀,将沉淀滤出,洗净烘干,其质量为9.850g。
48.滤液与酸作用不产生气体;若用足量的铵盐与滤液共热,则产生4.48L气体(标准状况),滤液中OH?的物质的量为_______mol。